El tretrafluoruro de xenón o cómo los gases nobles a veces no son tan nobles
2012-04-16
Los gases nobles suelen ser muy poco reactivos. En esencia, la reactividad química de una sustancia viene determinada por su configuración electrónica. Casi toda la química se reduce a las interacciones de los electrones más energéticos de distintos átomos y los gases nobles tienen estos electrones dispuestos de tal manera que no son favorables, en general, a la formación de compuestos químicos. Esto no quiere decir que sea físicamente imposible formar compuestos con gases nobles. Desde mediados del siglo XX, numerosos compuestos covalentes con gases nobles han sido sintetizados.
Se presenta el tetrafluoruro de xenón
Se acababa el verano de 1962 cuando Howard H. Claasen, Henry Selig y John G. Malm informaron de una síntesis muy audaz: nada menos que tetrafluoruro de xenón (XeF4). Compuestos como éste ya habían sido predichos sobre el papel muchos años antes y Neil Barlett había informado recientemente sobre la síntesis del hexafluoroplatinato de xenón (Xe+[PtF6]-). La existencia de esta última sustancia, el Xe+[PtF6]-, abría el camino a la preparación de auténticos compuestos con gases nobles, pero su descubrimiento en sí es materia para otro artículo, pues tiene muchos recovecos.
Volvamos al XeF4. Esta sustancia es un auténtico compuesto químico con sus buenos enlaces covalentes. Se considera que es el primer compuesto simple de gas noble en ser descubierto. Tiene geometría plana (sí, plana y no tetraédrica). En condiciones normales, es un sólido de color blanco y sublima a unos 390 K. Para la síntesis no hace falta recurrir a catalizadores especiales; basta con mezclar xenón y flúor molecular y elevar la temperatura a unos 670 K. Por supuesto, lo que sí hace falta es un contenedor capaz de resistir el ataque del flúor a tan alta temperatura.
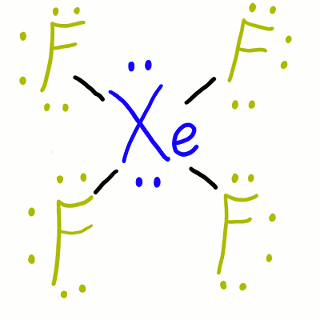
Representación de Lewis del tetrafluoruro de xenón.
Tras el descubrimiento del tetrafluoruro de xenón, llegaron otros compuestos simples. El xenón ha sido cortejado por elementos muy electronegativos como el flúor y el oxígeno en numerosas ocasiones. El flúor también ha conquistado el argón, el kriptón y el radón.
Categorías: Química
